
2020/3/13(金)、 日本循環器学会「2020年改訂版弁膜症治療のガイドライン」の内容をまとめました。2020/3/13(金)、日本循環器学会から6本のガイドラインのアップデートがありました。
→http://www.j-circ.or.jp/guideline/index.htm
日本循環器学会「2020年改訂版弁膜症治療のガイドライン」→http://www.j-circ.or.jp/guideline/pdf/JCS2020_Izumi_Eishi.pdf
この10年間の間に、大動脈弁狭窄症に対する経カテーテル大動脈弁留置術(transcatheter aortic valve implantation: TAVI)、僧帽弁閉鎖不全症に対する経皮的僧帽弁接合不全修復術、僧帽弁狭窄症に対する経皮的交連裂開術(Percutaneous transseptal mitral commissurotomy: PTMC)、生体弁置換後の弁機能不全に対して人工弁内人工弁挿入術(Valve in Valve)等のカテーテル治療の発展、日本人における手術適応や時期の推奨などについてアップデートされました。
【弁膜症の診断・評価法】
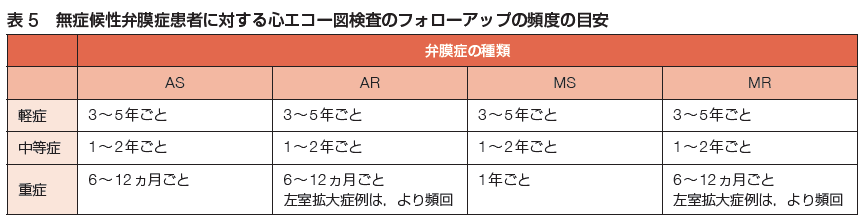
弁膜症の診断・評価法は、病歴、身体所見、生化学指標等がありますが、心エコー図検査が第一選択です。経胸壁心エコー図検査(TTE)は、弁膜症の診断においてもフォローアップにおいても最も重要な検査です。僧帽弁、大動脈弁、三尖弁、肺動脈弁それぞれに対して逆流と狭窄の有無、逆流症の評価としては、逆流ジェット面積、逆流ジェット縮流部(vena contracta)幅、有効逆流弁口面積(EROA)、逆流量 (regurgitant volume)、逆流率(regurgitant fraction)等の指標があり、狭窄症の評価としては、解剖学的弁口面積、機能的弁口面積、僧帽弁平均圧較差、圧半減時間、推定肺動脈収縮期圧等の指標があります。無症候性弁膜症患者に対する心エコー図検査のフォローアップの頻度の目安としては以下のような目安があります。原則1-2年ごとですが、重症の場合はフォローアップの期間を頻回にし、軽症の場合はフォローアップの期間を伸ばすと考えておくのが良いでしょう。他の検査としては必要に応じて、運動負荷心エコー、薬物負荷心エコー、経食道心エコー、非造影CT、冠動脈造影CT、非造影心臓MRI、造影心臓MRI、心臓カテーテル検査などがあります。
【僧帽弁閉鎖不全症/僧帽弁逆流症(MR)】
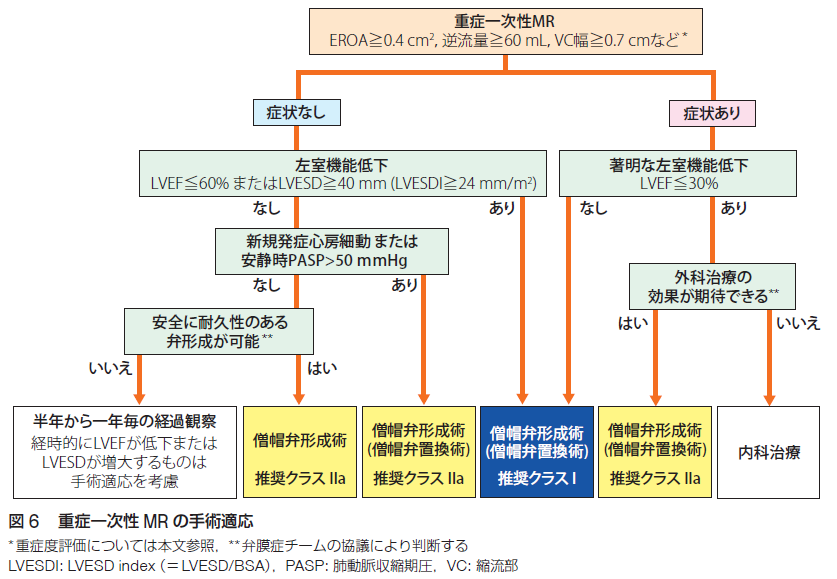
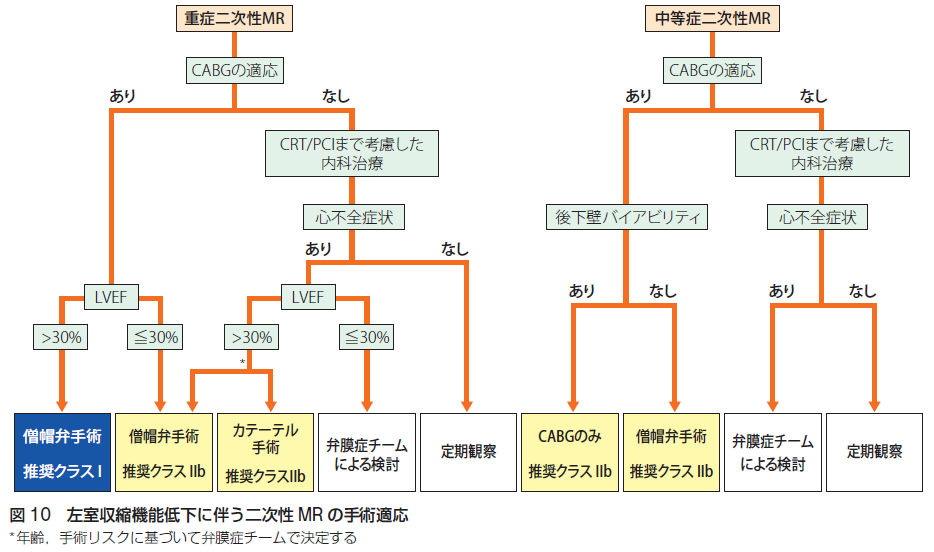
僧帽弁閉鎖不全症は、加齢による弁尖硬化、左室拡大、左室収縮力低下、心筋梗塞による乳頭筋断裂、変性による軸索断裂、感染性心内膜炎、リウマチ熱による弁尖硬化、心房細動、左房拡大による弁輪拡大、外傷性などが原因となります。重症度分類は心エコーによって、軽症、中等症、重症に分類します。逆流ジェットの左房面積に対する占有面積、有効逆流弁口面積、逆流量、逆流率、左房拡大の有無、左室拡大の有無を評価します。EROA0.4以上、逆流量60以上、VC幅0.7以上で重症と評価し、手術適応を考慮します。原則的に、症状があり、顕著な左室機能低下がなければ手術適応、顕著な左室機能低下があっても外科治療の効果が期待出来る場合も手術適応を考慮します。無症候性の場合は、左室機能低下があれば手術適応、左室機能低下がなくても新規発生心房細動または安静時肺動脈収縮期圧上昇ありの場合は手術適応、安全に耐久性のある弁形成が可能な場合も手術適応、それ以外の場合は手術適応なしと判断します。二次性僧帽弁閉鎖不全症(機能性僧帽弁閉鎖不全症)は、虚血性心疾患、拡張型心筋症、心臓サルコイドーシスに伴い発症します。CABGの適応、CRT/PCIの適応、心不全の有無、左室駆出率の程度、後下壁バイアビリティによって手術適応を判断します。僧帽弁閉鎖不全症に対する経皮的僧帽弁接合不全修復術、いわゆる「MitraClip」の適応は以下の通りです。手術適応を満たさない場合は経過観察(目安として軽症の場合3-5年、中等症の場合1-2年、重症の場合6-12ヶ月後の心エコーのフォロー)を行います。

【僧帽弁狭窄症(MS)】
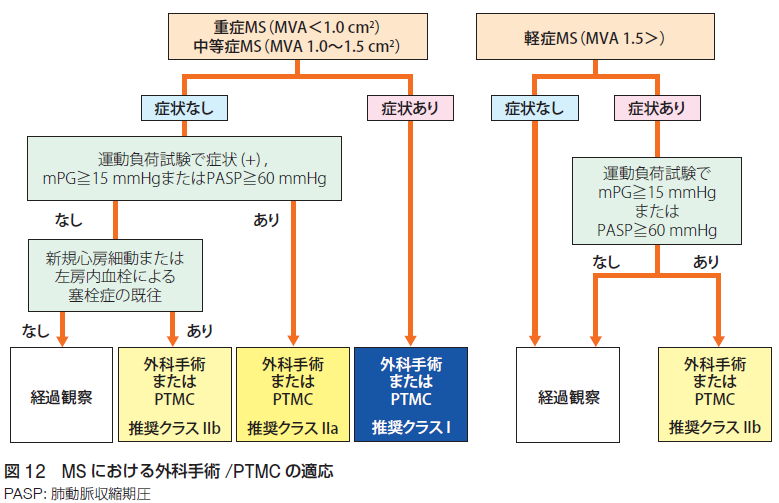
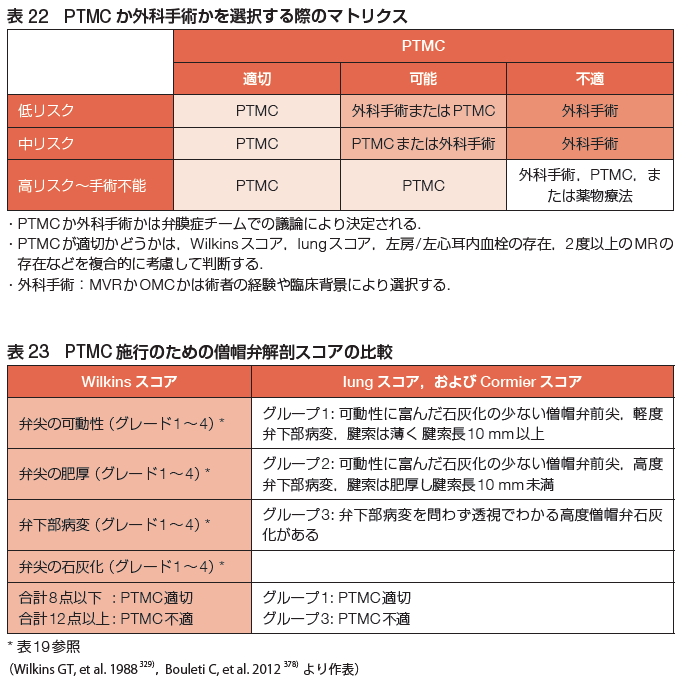
加齢による弁の硬化や石灰化、リウマチ熱、先天性心疾患によるものが原因です。僧帽弁狭窄症の重症度評価は、僧帽弁口面積(mitral valve area: MVA)、平均圧較差(mean pressure gradient: mPG)、拡張期圧較差半減時間(pressure half time: PHT)、特にMVAによって評価します。軽症MVA 2.0-1.5、中等症MVA 1.5-1.0、重症1.0未満と評価します。手術適応としては、重症または中等症の僧帽弁狭窄症で症状がある場合は手術適応、症状はなくても運動負荷試験で症状ありまたは平均圧較差15以上、肺動脈収縮期圧60以上、新規心房細動または左房内血栓による塞栓症の既往があれば手術適応と判断します。軽症の僧帽弁狭窄症は基本経過観察ですが、運動負荷試験で症状が出現または平均圧較差15以上、肺動脈収縮期圧60以上を認める場合は手術適応を考慮します。手術適応の場合は、僧帽弁狭窄症に対する手術は、経皮的交連裂開術(PTMC)または外科手術がありますが、 PTMCが可能かどうか、外科手術が可能かどうかで以下のように判断します。手術適応を満たさない場合は経過観察(目安として軽症の場合3-5年、中等症の場合1-2年、重症の場合6-12ヶ月後の心エコーのフォロー)を行います。
【大動脈弁閉鎖不全症/大動脈弁逆流症(AR)】
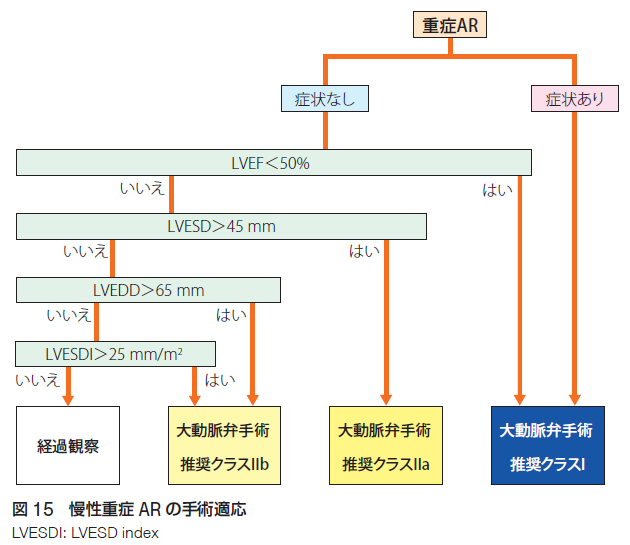
大動脈弁狭窄症は加齢による弁の変性や硬化、リウマチ性、先天性の弁異常、高血圧、大動脈解離、大動脈弁輪部拡張症、外傷性などが原因となります。大動脈弁狭窄症の重症度評価は逆流ジェットの大きさ(左室におけるジェット到達距離、ジェット幅)、逆流量、逆流率、有効弁口面積等の指標によって軽症、中等症、重症度と評価します。大動脈弁狭窄症の手術適応は比較的シンプルで心不全等の症状がある場合は早期の手術を推奨、症状がない場合も左室駆出率50未満の場合、左室収縮末期径(left ventricular end-systolic diameter: LVESD)45以上、左室拡張末期径(left ventricular end-diastolic diameter: LVEDD)65以上、LVESD index(LVESDを体表面積BSAで補正した指標)25以上で手術適応です。手術適応を満たさない場合は経過観察(目安として軽症の場合3-5年、中等症の場合1-2年、重症の場合6-12ヶ月後の心エコーのフォロー)を行います。
【大動脈弁狭窄症(AS)】
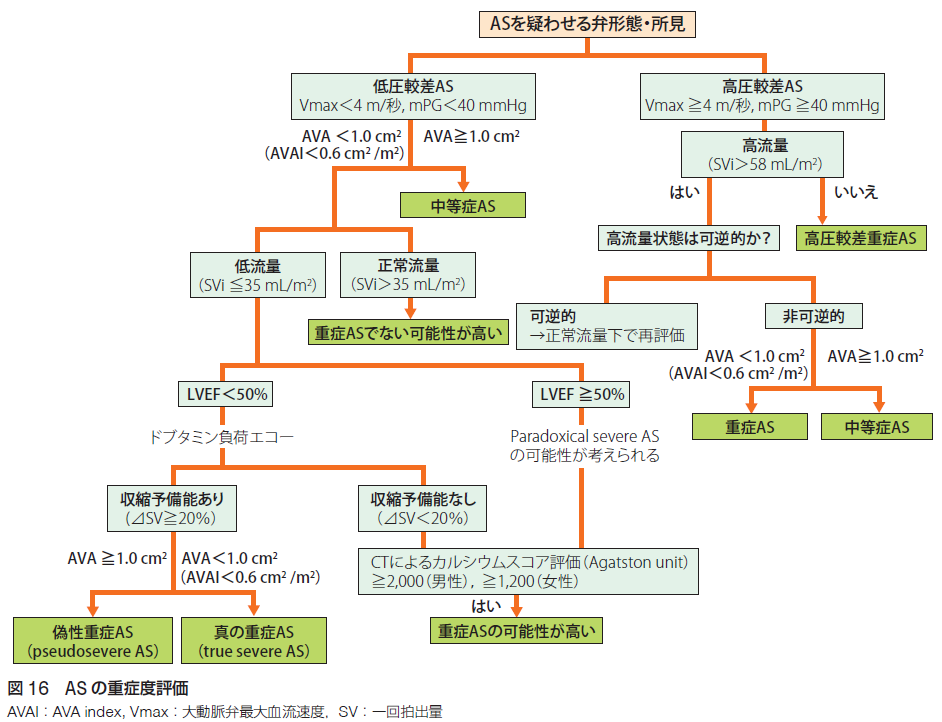
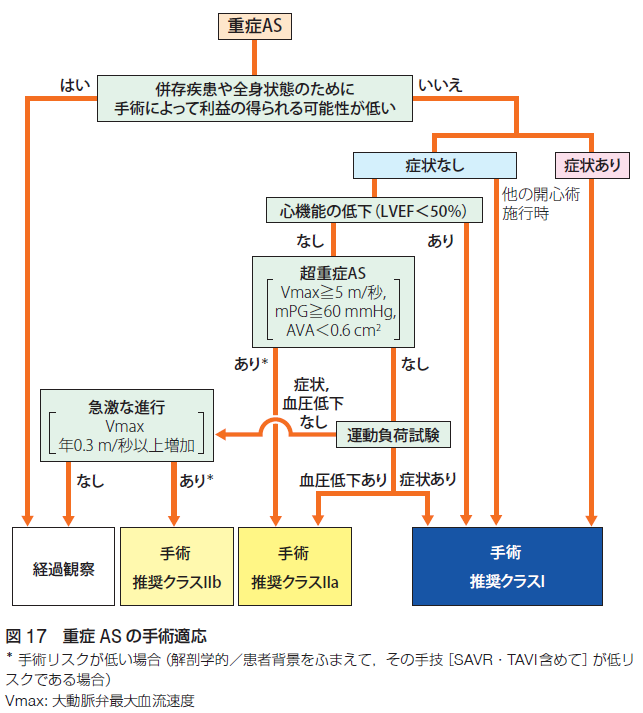
大動脈弁狭窄症の原因は加齢による弁の硬化が80%以上です。大動脈弁狭窄症はしばしば無症状で進行しますが、症状が出現した後では予後が悪いので早期発見が望まれます。大動脈弁狭窄症の重症度評価としては、大動脈弁の開放制限、大動脈弁口面積、大動脈弁最大血流速度、平均圧較差などの指標によって評価します。大動脈弁口面積1.0未満または体表面積で補正した大動脈弁口面積0.6未満で重症、大動脈弁口面積1.0以上で軽症または中等症です。大動脈弁最高血流速度4m/秒、平均圧較差40mmHg以上か以下かで高圧較差大動脈弁狭窄症か、低圧較差大動脈弁狭窄症かに分類します。少し複雑ですが下記をご覧ください。心不全症状、胸痛、失神等の症状の有無によって症候性と無症候性とに分類します。狭心症、心不全による呼吸困難、失神発作などを伴う有症候性の重症大動脈弁狭窄症は原則手術適応です。症状のない場合は、心機能低下、他の開心術施行時、超重症(Vmax 5m/秒以上、mPG 60以上、AVA0.6未満)の場合、運動負荷試験にて症状ありの場合は手術適応です。急激な進行(1年でVmax 0.3以上の進行)の場合も手術適応を考慮、それ以外の場合、併存疾患や全身状態のために手術によって利益の得られる可能性が低い場合は経過観察とします。手術適応を満たさない場合は経過観察(目安として軽症の場合3-5年、中等症の場合1-2年、重症の場合6-12ヶ月後の心エコーのフォロー)を行います。
【三尖弁閉鎖不全症/三尖弁逆流症(TR)】【三尖弁狭窄症(TS)】
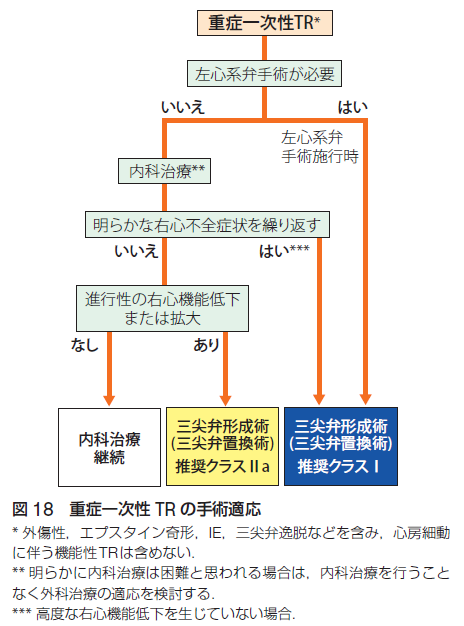
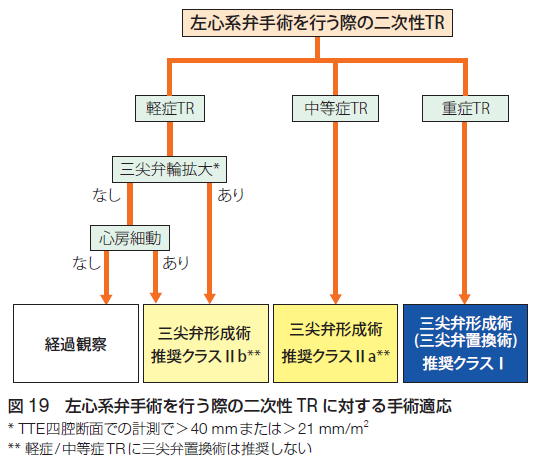
重症の三尖弁閉鎖不全症で、明らかな右心不全症状を繰り返す場合、進行性の右心機能低下または右心拡大を認める場合に手術適応を考慮します。左心系弁手術が必要な場合には合わせて治療を行う場合もあります。一方で、三尖弁狭窄症単独の手術は極めて稀ですが、有症状の重症三尖弁狭窄症に対して手術が考慮されることはあります。
【肺動脈弁閉鎖不全症(PR)】【肺動脈弁狭窄症(PS)】
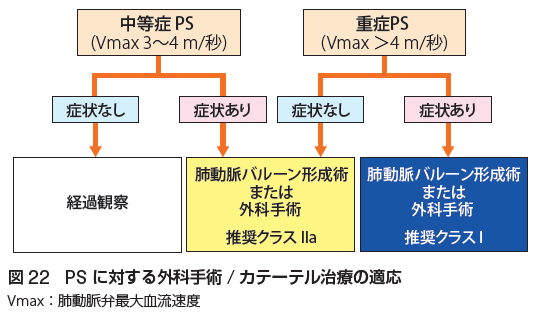
有症状の大動脈弁閉鎖不全症は手術適応、重症の肺動脈弁狭窄症、有症状の中等症の肺動脈弁狭窄症は手術適応、それ以外は経過観察です。
【連合弁膜症】
複数の弁膜症を合併していることを連合弁膜症と呼び、日本胸部外科学会の報告によると弁膜症手術のうち連合弁膜症の手術は28.2%を占めるとのことです。連合弁膜症手術で頻度が高いものは、三尖弁と左室弁の組み合わせで79.4%、僧帽弁と三尖弁が55.8%、大動脈弁と僧帽弁が20.6%、僧帽弁、大動脈弁、三尖弁の3弁15.9%です。また、大動脈弁狭窄症兼閉鎖不全症(ASR)、僧帽弁狭窄症兼閉鎖不全(MSR)のように同一の弁に狭窄症と閉鎖不全症が合併することもあります。左室系では、大動脈弁狭窄症(AS)兼僧帽弁逆流症 (MR)、大動脈弁閉鎖不全症(AR)兼僧帽弁閉鎖不全症(MR)、大動脈弁狭窄症(AS)兼僧帽弁狭窄症 (MS)があります。詳しくは日本循環器学会「2020年改訂版弁膜症治療のガイドライン」 をご覧ください。
日本循環器学会「2020年改訂版弁膜症治療のガイドライン」→http://www.j-circ.or.jp/guideline/pdf/JCS2020_Izumi_Eishi.pdf
【人工弁置換術後】
人工弁には機械弁と生体弁があります。機械弁は耐久性に優れていますが、生涯に渡った抗凝固療法が必須で、生体弁は抗凝固療法は必須ではないが、耐久性に問題がある場合がありますが、どちらも技術の進歩によって改善されて来ています。人工弁例に対する抗血栓療法としては、ワルファリンのみが適応です。アスピリンやDOACは推奨されていません。ワルファリンのコントロールの目安は以下の通りです。
ワルファリンによる永続的な抗凝固療法(推奨クラスI、エビデンスレベルB)
ワルファリンコントロールのPT-INRの目安:
・大動脈弁:PT-INR 2.0-2.5
・大動脈弁位かつ塞栓症リスク有り:PT-INR 2.0-3.0
・僧帽弁:PT-INR 2.0-3.0
・適切な抗凝固療法中であっても明らかな血栓塞栓症を発症した患者に対するINR 2.5-3.5 を目標としたワルファリン投与(推奨クラスIIa、エビデンスレベルC)
・適切な抗凝固療法中であっても明らかな血栓塞栓症を発症した患者に対するアスピリンの併用(推奨クラスIIa、エビデンスレベルC)
・アスピリン単独投与(推奨クラスIII、エビデンスレベルB)
・DOACの使用(推奨クラスIII、エビデンスレベルC)
他に、観血的処置時の抗血栓薬の中止、血栓弁、人工弁機能不全などが記載されています。
【弁形成術後】
僧帽弁形成術後のフォローアップと再手術の適応、大動脈弁形成術(AVP)・自己弁温存基部置換術後のフォローアップと再手術の適応などが記載されています。
【合併する心房細動に対する治療】
心房細動は弁膜症生心房細動と非弁膜症性心房細動があります。全ての弁膜症が弁膜症性ではなく、日本循環器学会「2020年改訂版弁膜症治療のガイドライン」では「中等症以上のMSと機械弁」を「弁膜症性」と定義されています。弁膜症性心房細動では特に塞栓症のリスクが高いため、PT-INR 2.0-3.0でのワルファリン療法が推奨されています。弁膜症性心房細動にDOACの適応はありませんが、生体弁置換術後の心房細動にDOACは使用することがあります。弁膜症手術時におけるMaze手術、左心耳閉鎖、左心耳切除術の適応を考慮します。
【冠動脈疾患合併弁膜症】
冠動脈疾患と弁膜症を合併している頻度は高齢化に伴って多く、日本胸部外科学会の調査によると、弁膜症手術例におけるCABG同時手術は2009年には19.8%を占めるとのことです。大動脈弁手術時の血行再建、CABG施行時の弁膜症手術も可能であれば同時手術が推奨されるとのことです。
その他、妊娠の弁膜症、マルファン症候群、感染性心内膜炎の予防、リウマチ熱の予防など記載があります。詳しくは日本循環器学会「2020年改訂版弁膜症治療のガイドライン」 をご覧ください。
日本循環器学会「2020年改訂版弁膜症治療のガイドライン」→http://www.j-circ.or.jp/guideline/pdf/JCS2020_Izumi_Eishi.pdf

